客户文章丨Molecules血清中肉碱与心衰
心力衰竭(HF)仍然是世界范围内的主要心脏疾病和公共卫生负担,目前可行的预测因素主要包括左心室射血分数(LVEF)、利钠肽水平和纽约心脏病学会(NYHA)的心衰分级,但是这些依旧不能完全解释和预测慢性HF患者长期不良发生的风险。代谢组学技术在临床研究中显现出作为诊断/预测工具和优化管理的潜力,众所周知,心力衰竭进展过程中会发生代谢功能障碍,心肌中脂肪酸减少,脂肪酸氧化需要通过肉碱穿梭往线粒体内运输,推测这个过程可能在HF进展中起着关键作用。复旦大学附属中山医院葛均波团队、钱菊英团队和复旦大学人类表型组研究院唐惠儒团队合作,于2023年在Molecules期刊上发表题为“Quantitative Profiling of Serum Carnitines Facilitates the Etiology Diagnosis and Prognosis Prediction in Heart Failure”的研究论文,发现脂酰肉碱不仅可用于HF诊断,也可以用于非缺血性扩张型心衰(DCM-HF)的诊断,还可以用于预测不良发生。原文链接:https://doi.org/10.3390/molecules28145345,我公司参与了该研究中脂酰肉碱检测方法的开发和样品的定量检测工作。

01 实验设计
筛选入组的志愿者共有209名,其中非缺血性扩张型心衰(DCM-HF)病人98名,缺血型心衰(IHD-HF)病人63名,健康对照组48名。对这三组志愿者的血清定量检测脂酰肉碱水平。
HF病人均满足:NYHA分级至少Ⅱ级、LVEF<55%、NT-pro-BNP>125 pg/ml这三个条件。基线特征表明:DCM-HF组和IHD-HF组的病人心脏功能与对照组相比差得多,而且DCM-HF组的病人与IHD-HF组相比,LVEF更低而左心房直径更高。

02 结果
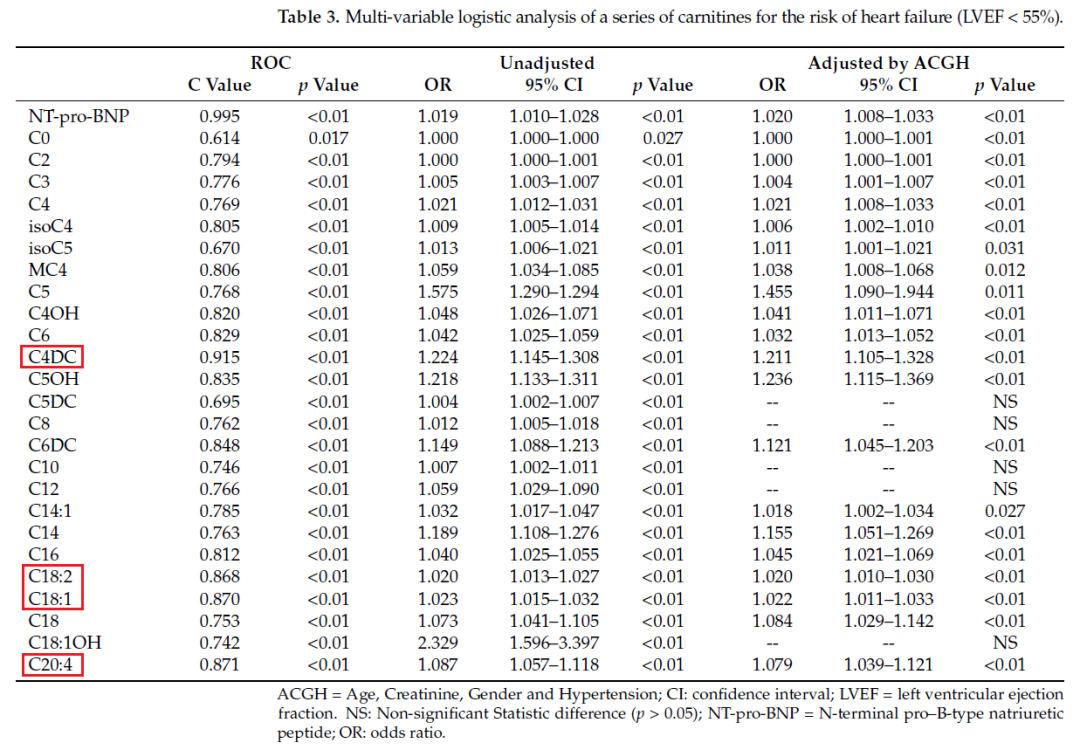
将HF与对照组进行比较,发现4种脂酰肉碱C4DC(AUC = 0.915,p < 0.01)、C20:4(AUC = 0.871,p < 0.01)、C18:1(AUC = 0.870,p < 0.01)和 C18:2 具有显着值 (AUC = 0.868,p < 0.01),并且发现年龄、性别、高血压和血清肌酐独立地增加了心力衰竭的诊断。评估了每种肉碱对HF诊断的独立影响,同时根据上述因素调整,证明了这4种肉碱可以独立验证心力衰竭诊断,如表 3 所示。
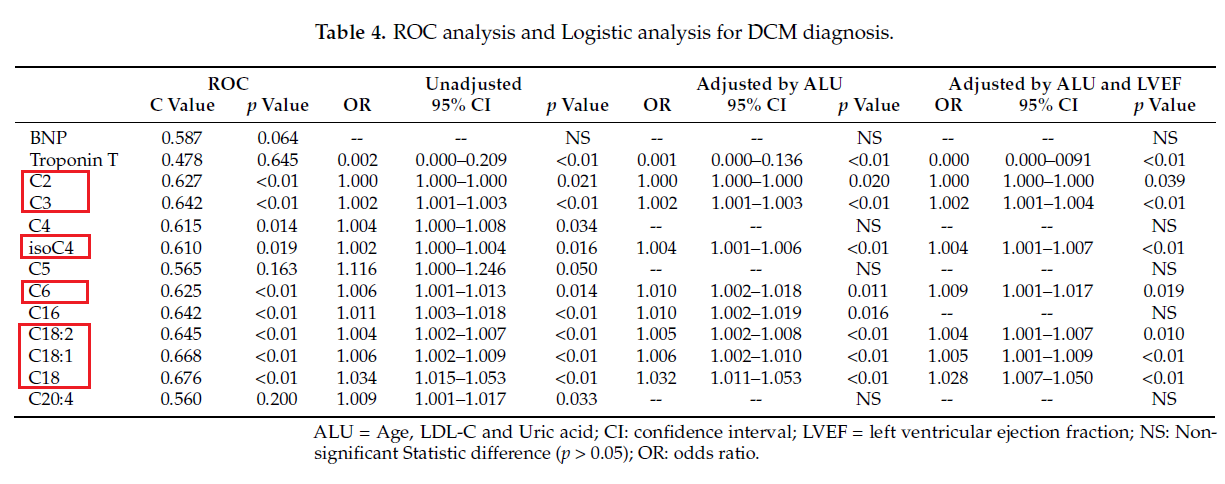
进一步地,即使调整年龄、LDL-C、血尿酸和 LVEF,发现7种脂酰肉碱能诊断DCM-HF,这7种脂酰肉碱是C2、C3、isoC4、C6、C18、C18:1和C18:2,如表4所示。
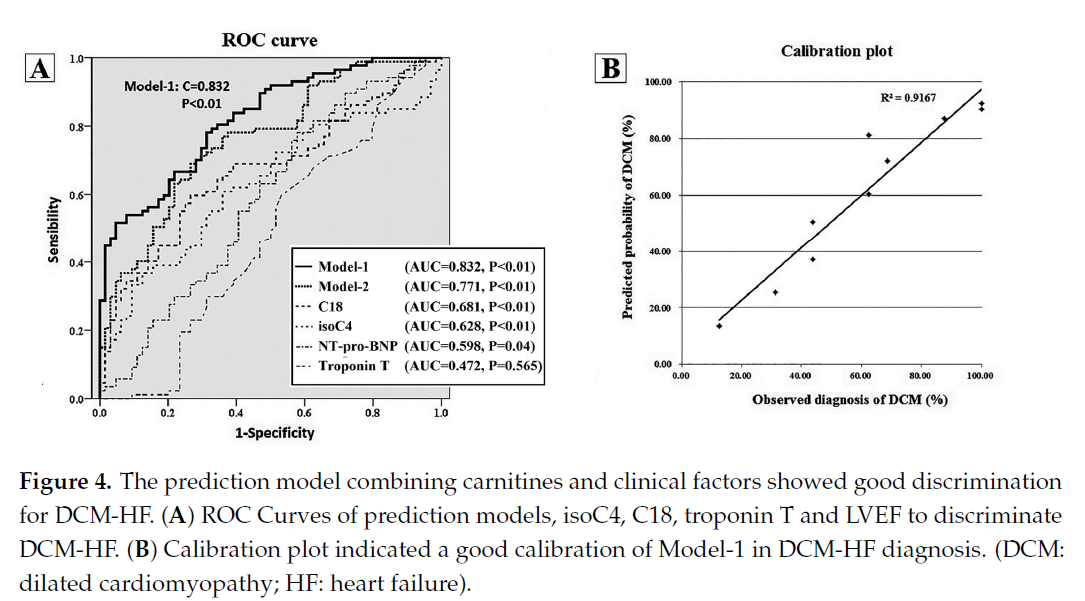
最终,结合临床指标,我们认为使用isoC4、C18、troponin T和LVEF能较好诊断DCM-HF,如图4所示。
在随访的 28.3个月(中位数)期间,12 名患者失访,总共发生 43例死亡事件,其中IHD-HF组死亡18 例(31.6%),DCM-HF组死亡 25例(27.2%),还有54例HF患者(14例IHD-HF,40例DCM-HF)再次住院。
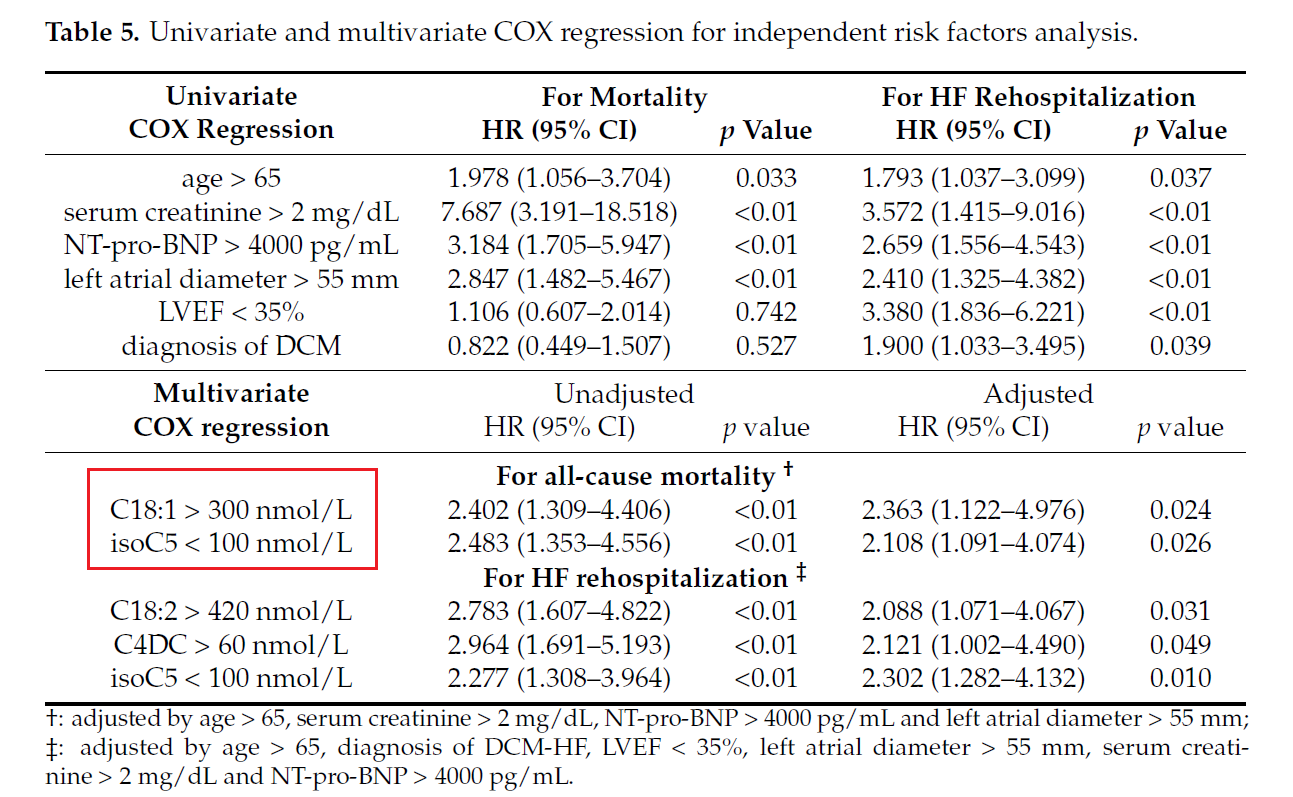
对全因死亡率的分析发现,除了年龄(> 65岁)、血肌酐(> 2 mg/dL)、NT-pro-BNP(> 4000 pg/mL)、左心房直径(> 55 mm)这些高危因素外,C18:1和isoC5也会增加全因死亡率,如表5所示。
03 检测方法
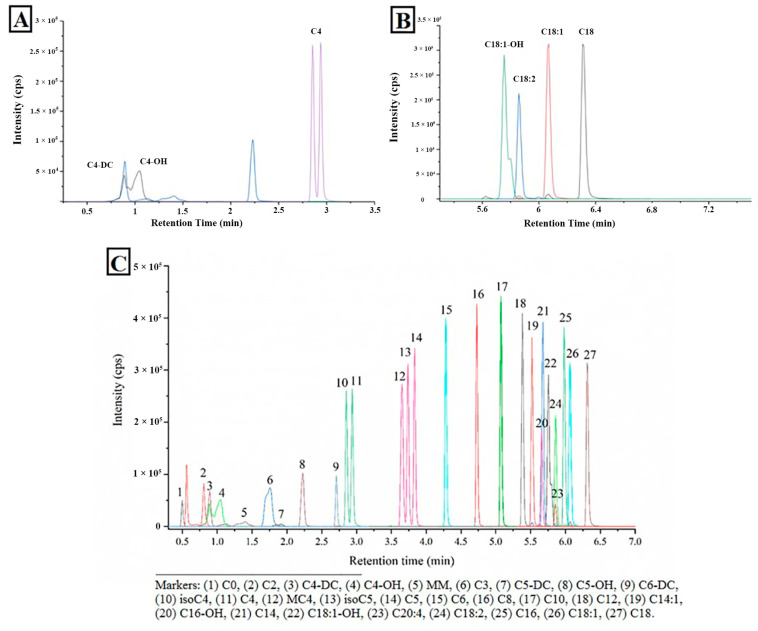
使用超高效液相色谱-质谱联用仪(1290-6470 UPLC-MS/MS,Agilent)对血清中脂酰肉碱进行定量检测,使用内标法定量。
04 讨论
在本研究中,我们证实了HF患者血清中有几种脂酰肉碱显著增加,并且与不良的长期预后独立相关。更有趣的是,我们验证了脂酰肉碱能有效区分DCM 和 IHD 的诊断能力。据我们所知,迄今为止尚未有相关报道。
作为运输长链脂肪酸的重要载体,脂酰肉碱水平及其变化直接影响线粒体脂肪酸的氧化效率。相反,HF中脂肪酸代谢的不可逆重塑也会干扰脂酰肉碱的合成。因此,循环脂酰肉碱的浓度与心衰的疾病分型、预后相关是有机制基础的。
延伸阅读
脂酰肉碱:人体内的肉碱可以通过饮食(富含于红肉)得到补充,也可以通过生物合成的方式从赖氨酸(Lys)及蛋氨酸(Met)产生。肉碱在能量代谢中起着非常重要的作用,是转运脂肪酸的载体,特别是对于大部分能量都来自于脂肪酸氧化的心脏和骨骼肌。
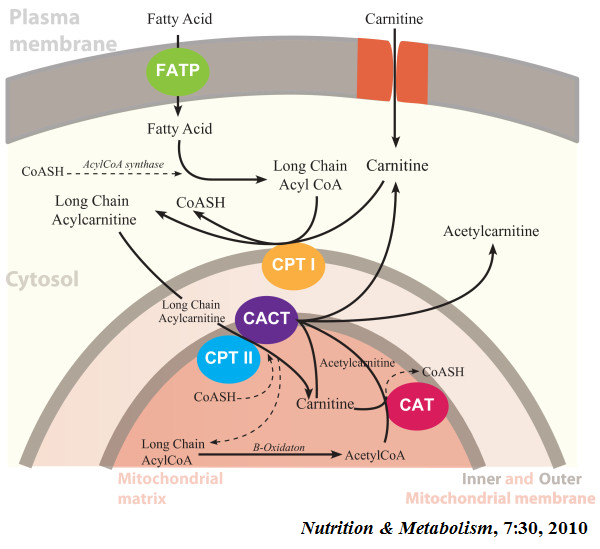
肉碱穿梭和脂肪酸氧化:由于脂肪酸活化成脂酰CoA发生在胞液中,而脂肪酸氧化发生在线粒体基质内,中短链脂酰CoA可以渗透通过线粒体内膜,而长链脂酰CoA不能通过,需要一个特殊的运输机制-肉碱穿羧系统(Carnitine shuttle system)。肉碱脂酰转移酶I(CPT I)位于线粒体外膜上,使得脂酰CoA(Acyl-CoAs)变成了脂酰肉碱(Acylcarnitines);位于线粒体内膜上的肉碱-脂酰肉碱转移酶(CACT)将脂酰肉碱顺利转运至线粒体基质中;脂酰肉碱一旦进入到线粒体基质,就在肉碱脂酰转移酶II(CPT II)作用下释放出游离肉碱,形成的脂酰CoA进行脂肪酸β氧化变成乙酰CoA;游离的肉碱一部分可以通过CACT转移到线粒体外,一部分还可以和乙酰CoA在肉碱转移酶(CAT)作用下生成CoA和乙酰肉碱,乙酰肉碱也可以通过CACT转移到线粒体外。
肉碱与遗传性代谢缺陷疾病:由于某些酶的基因位点发生突变,会造成肉碱由细胞外转运至细胞内的能力下降,胞浆内肉碱浓度降低,尿肉碱丢失增加,血清肉碱浓度降低,长链脂肪酸在细胞质中积聚,引起代谢紊乱和多脏器损伤,被称为原发性肉碱缺乏症。针对新生儿的脂肪酸及酰基肉碱的浓度检查,能筛查出这部分的遗传性代谢缺陷患儿,并进行及早干预。



